Estados físicos da matéria – O que são? Quais são? Transformações
A matéria pode ser classificada de duas maneiras: de acordo com seu estado físico e de acordo com sua composição.
Se for classificada de acordo com sua composição, dizemos que ela é um elemento, um composto ou uma mistura. Já a sua classificação de acordo com seu estado físico é o que veremos a seguir.
Estados físicos da matéria: o que são?
Os três estados físicos da matéria são: líquido, sólido e gasoso. Todos possuem diferenças visíveis, pois geralmente sabemos identificar em qual estado físico está uma substância.
Por exemplo, vamos analisar como vemos a água nos seus três estados físicos. Quando a colocamos em uma forma e deixamos esse recipiente por um tempo no congelador, ocorre um processo de solidificação, e a água em estado líquido vai para seu estado sólido, que é conhecido como gelo.
A água que sai das torneiras de nossa casa está no estado líquido, pois ela acaba se adaptando à forma do recipiente no qual a colocamos.
Se dispomos essa água para aquecer no fogão, veremos que aos poucos ela vai se tornando um vapor que vai para o ambiente. Portanto, ela está em seu estado gasoso.
Estado gasoso
Um gás, também conhecido como vapor, não tem volume nem forma definida, ou seja, ele assume o volume ou a forma do recipiente que o contém. Um gás pode ser comprimido, para ocupar um volume menor, ou pode ser expandido, para ocupar um volume maior.
Nesse estado, as moléculas estão muito distantes umas das outras e movem-se com velocidade muito altas, colidindo repetidamente entre si e contra as paredes do recipiente.
Estado líquido
Um líquido tem volume definido, independente do recipiente que ele ocupa, portanto, ele não pode ser comprimido como os gases podem.
As moléculas de um líquido são mais empacotadas, ou seja, elas se movem rapidamente de um modo que conseguem desviar uma das outras, mas não tão rápidas quanto as moléculas de uma substância em estado gasoso.
Estado sólido
Um sólido tem tanto forma quanto volume definidos, porque ele é rígido. Portanto, ao contrário de um gás, ele não pode ser comprimido.
Nesse caso, as moléculas estão presas entre si, geralmente com arranjos definidos, nos quais elas podem apenas oscilar superficialmente em suas posições fixas. Com isso, é possível então entender porque os sólidos têm formas rígidas.
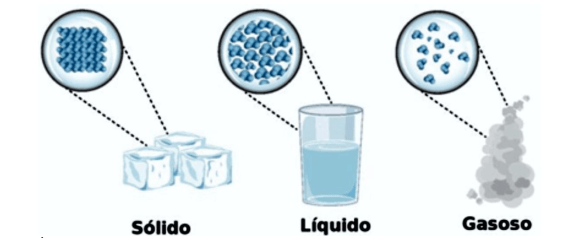
A visão molecular mostra que as moléculas no estado sólido são arranjadas de maneira mais ordenada do que as no estado líquido. As moléculas no gás estão muito mais separadas do que no líquido ou sólido.
Diferenças e semelhanças entre os estados físicos da matéria
Nos líquidos, as forças atrativas intermoleculares são fortes o suficiente para manter as moléculas juntas. Isso faz com que os líquidos sejam muito mais densos e muito menos compressíveis que os gases.
Entretanto, as forças atrativas nos líquidos não são tão fortes para impedir que as moléculas se movimentem próximas às outras. Assim, os líquidos podem ser derramados e assumirem a forma do recipiente, algo que não ocorre com os sólidos que são rígidos (como o gelo é, por exemplo).
Nos sólidos, as forças atrativas intermoleculares são fortes para manter as moléculas juntas e “prende-las” no lugar. Os sólidos, como os líquidos, não são muito mais compressíveis porque as moléculas têm pouco espaço livre entre elas. Geralmente, as moléculas assumem um padrão altamente regular, que são as estruturas chamadas cristalinos. E como as partículas não são livres, não sofrem movimentos, sendo substâncias no estado sólido mais rígidas.
Nível molecular de substâncias em diferentes estados físicos
O estado de uma substância depende da energia cinética e das energias de atração entre as partículas.
As energias cinéticas dependem da temperatura, tendem a manter as partículas separadas e em movimento. As atrações entre as partículas, de modo contrário à ação da energia cinética, tendem a deixá-las juntas.
As substâncias gasosas à temperatura ambiente têm atrações mais fracas que as líquidas e estas têm atrações mais fracas que as sólidas.
Resumindo:
- Gás: desordem total das partículas, muitos espaços vazios, partículas têm liberdade de movimento e ficam muito separadas;
- Líquido: desordem, as partículas ou aglomerados de partículas estão livres para se mover umas em relação às outras e as partículas estão próximas;
- Sólido: arranjo ordenado, as partículas estão basicamente em posições fixas e estão muito próximas.
Estados físicos da água
Os três estados físicos da água são vapor de água, água líquida e gelo.
Não podemos ver o vapor de água. O que vemos quando olhamos para a fumaça ou para as nuvens são gotas minúsculas de água líquida dispersas na atmosfera.
Porém, os estados líquidos e sólidos da água nós podemos ver a olho nu.








Deixe seu comentário